A qualidade do laudo anátomo-patológico e citopatológico depende de uma série de fatores, tais como: fornecimento de dados clínicos completos, coleta e transporte adequados, descrição macroscópica, correta fixação dos tecidos e dos esfregaços, emblocamento em posição ideal dos cortes histológicos, coloração das lâminas e, finalmente, interpretação pelo patologista.
Qualquer elo rompido nesta cadeia poderá prejudicar a exatidão e a prontidão do resultado. Por essa razão, o Instituto Moacyr Junqueira (IMJ), através destas instruções, oferece os subsídios necessários para a obtenção, preservação e transporte adequados do material a ser examinado.
Este POP foi elaborado para atender às diretrizes das RDCs 504/21, 786/23 e 978/25 da ANVISA, abrangendo todos os aspectos de coleta, acondicionamento, transporte, rastreabilidade e recebimento do Material Biológico Humano (MBH).
O objetivo destas informações é instruir todos os envolvidos (remetente, transportador, destinatário) quanto aos métodos de envio e transporte dos exames anátomo-patológicos e citopatológicos, minimizando riscos e assegurando a qualidade das amostras para diagnósticos precisos.
O documento detalha as etapas de rastreabilidade, revalidação periódica do acondicionamento e armazenamento dos registros de transporte por, no mínimo, cinco anos, conforme exigido pela legislação vigente.
Este procedimento também contempla os requisitos de qualificação das embalagens primárias, secundárias e terciárias, validação de transporte, gestão de incidentes e acidentes, e implementação de controles que assegurem a rastreabilidade integral das amostras e materiais correlatos em todas as etapas, conforme o disposto na RDC 978/2025, que reforça a necessidade de manutenção da integridade, identidade e segurança do MBH desde a origem até o destino final.
O IMJ adota metodologia documentada para qualificação dos meios de transporte e de acondicionamento, incluindo a verificação da conformidade das embalagens, a rastreabilidade por meio de etiquetas, registros digitais e o uso de tags de monitoramento, conforme aplicável.
Este POP reflete também o princípio de biossegurança e integridade amostral descrito na nova resolução, incorporando as exigências de qualificação de fornecedores, controle ambiental e rastreabilidade eletrônica das remessas.
Estabelecer as instruções padronizadas para a coleta, acondicionamento, transporte, rastreabilidade e recebimento de materiais biológicos humanos destinados a exames anátomo-patológicos e citopatológicos, assegurando a qualidade, integridade e segurança das amostras encaminhadas ao IMJ.
Garantir que todos os processos envolvidos no transporte e manipulação de MBH estejam em conformidade com as exigências da ANVISA e com os requisitos legais vigentes, de modo a prevenir não conformidades e assegurar resultados diagnósticos confiáveis.
O presente procedimento também tem por objetivo garantir a qualificação e validação contínua dos processos de transporte e acondicionamento, incluindo os critérios de aceitação, verificação periódica dos recipientes e controle dos parâmetros críticos que possam interferir na estabilidade e integridade do MBH.
Define ainda os parâmetros de rastreabilidade e comunicação entre remetente, transportador e destinatário, conforme requisitos de desempenho, segurança e integridade amostral previstos na RDC 978/2025.
Este Procedimento Operacional Padrão aplica-se a todos os profissionais envolvidos nas etapas de coleta, acondicionamento, transporte e recebimento de material biológico humano (MBH) para exames anatomopatológicos, incluindo representantes externos, motoboy, equipe de triagem/conferência e recepção técnica do Instituto Moacyr Junqueira.
Abrange as unidades de saúde conveniadas (consultórios, clínicas e hospitais), bem como os setores internos responsáveis pelo controle de qualidade, rastreabilidade e recepção das amostras, assegurando o cumprimento das boas práticas estabelecidas pelas Resoluções RDC nº 504/2021, nº 786/2023 e nº 978/2025 da ANVISA.
No escopo deste procedimento, as responsabilidades específicas estão assim definidas:
• Remetente: Responsável pelo correto acondicionamento do MBH, identificação e rotulagem dos frascos conforme exigido, preenchimento da documentação de expedição e comunicação prévia (requisição médica e/ou formulário institucional) e pela comunicação prévia ao destinatário sobre qualquer informação relevante da amostra.
• Representante Externo: Responsável pelo transporte adequado das amostras, zelando pela integridade do material durante todo o trajeto. Deve verificar o cumprimento dos requisitos de rotulagem, acondicionamento e identificação no momento da coleta, além de realizar a higienização dos recipientes de transporte conforme os protocolos de biossegurança estabelecidos.
• Destinatário (Instituto Moacyr Junqueira): Responsável por inspecionar e registrar as condições do MBH no momento do recebimento, conferindo documentação, identificação e integridade das amostras. Deve comunicar ao remetente a chegada do material e relatar imediatamente qualquer inconformidade observada.
| Responsável | Atividade |
| Representante / Motoboy | Coletar MBH com todos os dados necessários e acondicionar conforme instruções. |
| Cliente (Unidade de Saúde) | Providenciar o envio adequado do material conforme orientação prévia. |
| Transportador – IMJ | Zelar pela integridade da embalagem e garantir o transporte nas condições adequadas. |
| Recebimento – IMJ | Conferir documentação e integridade da amostra, registrar entrada. |
| Laboratório IMJ | Rastrear material no sistema e realizar conferência técnica do recebimento. |
Este POP também se aplica aos fornecedores e parceiros eventuais do IMJ, bem como aos colaboradores responsáveis pela coleta e transporte interno de material biológico humano, que devem seguir integralmente as instruções descritas neste documento, além das exigências de qualificação, validação e biossegurança previstas na RDC 978/2025. O IMJ assegura que todos os colaboradores designados para coleta e transporte são devidamente capacitados, qualificados e monitorados quanto ao cumprimento das normas vigentes, de acordo com o Programa de Treinamento Interno e o Sistema de Gestão da Qualidade.
O Instituto Moacyr Junqueira (IMJ) é classificado como Laboratório de Anatomia Patológica e Citopatologia, conforme estabelecido pela RDC nº 978/2025 da ANVISA, possuindo estrutura física, técnica e organizacional adequada para a execução de atividades de coleta, acondicionamento, transporte, processamento técnico e emissão de laudos anatomopatológicos e citológicos.
O escopo técnico do serviço abrange o recebimento e processamento de amostras biológicas humanas (MBH) provenientes de procedimentos ambulatoriais e hospitalares, incluindo biópsias, peças cirúrgicas, materiais citológicos e amostras para exames de imuno-histoquímica e estudos complementares.
O IMJ é responsável técnico por todas as etapas do processo descritas neste procedimento, incluindo:
• Recebimento e conferência do material biológico;
• Processamento técnico das amostras;
• Análise microscópica e emissão dos laudos;
• Armazenamento e arquivamento de lâminas, blocos e registros;
• Gestão da rastreabilidade e controle da qualidade.
Conforme previsto na RDC nº 978/2025, as atividades terceirizadas estão restritas a etapas analíticas específicas, com vínculo contratual formalizado e responsabilidade compartilhada supervisionada pelo Responsável Técnico do IMJ. Atualmente, o IMJ mantém contrato técnico de prestação de serviços com o CEH (Centro Especializado de Histotecnologia), responsável pela confecção de lâminas e reações imuno-histoquímicas sob supervisão direta do IMJ.
Todos os prestadores externos são qualificados e monitorados periodicamente, mediante critérios técnicos e documentais definidos pelo Sistema de Gestão da Qualidade, incluindo:
• Análise de desempenho técnico e documental;
• Auditorias e avaliações de conformidade;
• Registros de qualificação e requalificação;
• Controle de rastreabilidade das amostras e resultados.
O vínculo contratual com cada prestador de serviço contempla cláusulas específicas sobre:
• Responsabilidade técnica e ética;
• Garantia da rastreabilidade e integridade das amostras;
• Manutenção da confidencialidade dos dados;
• Cumprimento das exigências legais e sanitárias vigentes.
O IMJ mantém arquivados os contratos, relatórios de auditoria e evidências de qualificação de todos os prestadores e fornecedores de serviços terceirizados, conforme os requisitos estabelecidos no Sistema de Gestão da Qualidade e na RDC 978/2025.
A qualidade do laudo anátomo-patológico e citopatológico depende de uma série de fatores, tais como: fornecimento de dados clínicos completos, coleta e transporte adequados, descrição macroscópica, correta fixação dos tecidos e dos esfregaços, emblocamento em posição ideal dos cortes histológicos, coloração das lâminas e, finalmente, interpretação pelo patologista. Qualquer elo rompido nesta cadeia poderá prejudicar a exatidão e a prontidão do resultado.
Por essa razão, o Instituto Moacyr Junqueira, através destas instruções, oferece os subsídios necessários para a obtenção, preservação e transporte adequados do material a ser examinado.
Este POP foi elaborado para atender às diretrizes das RDCs nº 504/2021, nº 786/2023 e nº 978/2025 da ANVISA, abrangendo todos os aspectos de coleta, acondicionamento, transporte e recebimento do Material Biológico Humano (MBH).
O objetivo destas informações é instruir todos os envolvidos (remetente, transportador e destinatário) quanto aos métodos de envio e transporte dos exames anátomo-patológicos e citopatológicos, minimizando riscos e assegurando a qualidade das amostras para diagnósticos precisos.
O documento detalha as etapas de rastreabilidade, revalidação periódica do acondicionamento, controle de temperatura, qualificação de embalagens, procedimentos de contingência e armazenamento dos registros de transporte por, no mínimo, cinco anos, conforme exigido pela legislação.
Anátomo Patológico: Como regra geral, os frascos para anatomia patológica devem ser grandes e de boca larga para permitir a fácil colocação e retirada do material, além de conter a quantidade suficiente de fixador (recomendado dez vezes o volume do material a ser fixado para amostras pequenas). O tempo e a velocidade de penetração nos tecidos e fixação são lentos; portanto, em materiais volumosos, sugere-se secção para melhor fixação. Lembramos que o fixador endurece o material, e vidros pequenos e rígidos podem alterar a forma da peça cirúrgica. As peças grandes devem ser colocadas em sacos plásticos firmes e bem vedados, de preferência com embalagem dupla para evitar vazamentos, ou em frascos grandes.
Citopatológico: Os frascos utilizados para citopatologia têm tamanho e formato específicos, com ranhuras que permitem o acondicionamento de no mínimo três lâminas sem contato entre elas.
Revisão: Lâminas e blocos para revisão e/ou imuno-histoquímica devem ser armazenados em recipientes rígidos para evitar quebra. Não há necessidade de solução fixadora nesses casos, mas deve-se evitar exposição direta ao sol. Para transporte, colocar em um recipiente secundário e, em seguida, em uma caixa devidamente identificada.


Os materiais devem ser acondicionados terciariamente em um recipiente rígido e lavável, identificado conforme a legislação, para transporte seguro até o laboratório. Esses recipientes devem ser submetidos a uma limpeza regular com álcool 70% (diariamente ou semanalmente). Em situações especiais (por exemplo, derramamentos), o recipiente terciário deve ser lavado com água corrente e detergente clorado. A rotulagem da embalagem terciária deve incluir:
• Identificação completa do remetente e destinatário, com endereços e telefones de contato.
• Identificação do tipo de MBH.
• Etiquetas de advertência, modo e sentido de abertura, quando aplicável.
• Contatos telefônicos de emergência 24 horas para acidentes e incidentes.
Conforme a RDC 978/2025, as embalagens utilizadas para transporte devem ser qualificadas e revalidadas periodicamente, garantindo sua integridade, impermeabilidade e desempenho em diferentes condições de temperatura e umidade.
A embalagem terciária deve ser dotada de identificação “substância biológica categoria B – UN 3373”. O IMJ mantém registros de qualificação, revalidação e rastreabilidade dos recipientes e das etiquetas utilizadas.
Como regra geral, o fixador universal é a formalina a 10% tamponada. Deve-se diluir 1 litro de formalina pura para 9 litros de água (preferencialmente destilada). A amostra coletada e fixada em formol deve ser enviada ao laboratório em até 12-48 horas, para evitar alterações indesejadas. Todo material coletado deve ser fixado em formol 10% tamponado, exceto biópsias retais para oograma, que devem ser enviadas em soro fisiológico. O volume do fixador nos frascos deve ser de no mínimo 10x o volume do material.
Observação: o material coletado e fixado deve ser enviado ao laboratório no prazo de até 72 horas, preferencialmente. Material enviado além deste prazo não inviabiliza o procedimento, mas pode gerar artefatos pré-analíticos de hiperfixação com potencial risco de alterar o resultado dos exames subsequentes de imuno-histoquímica e/ou testes moleculares, caso necessários. Data e hora da coleta devem ser registradas na requisição de exames.
Exames pré-operatórios (congelação) devem ser acondicionadas em frasco sem solução fixadora e enviadas imediatamente ao laboratório.
Citopatologia Cérvico-Vaginal: Como regra, o fixador para lâminas de citologia é o álcool etílico a 96%. O material deve ser fixado imediatamente após a coleta para evitar artefatos de ressecamento. O spray fixador também pode ser usado logo após a coleta.
Observação: o material coletado e fixado deve ser enviado ao laboratório no prazo de até 48 horas, preferencialmente. Material enviado além deste prazo não inviabiliza o procedimento, mas pode gerar artefatos pré analíticos que potencial risco de alterar o procedimento ou exames subsequentes.
Citopatologia de PAAF: Como regra, o fixador para lâminas de citologia é o álcool etílico a 96%. O material deve ser fixado imediatamente após a coleta para evitar artefatos de ressecamento. O spray fixador também pode ser usado logo após a coleta. Em casos específicos, a lâmina pode ser enviada seca, dentro dos frascos com ranhura, mas deve ser devidamente identificada para uso de corantes específicos (giemsa).
Observação: o material coletado e fixado deve ser enviado ao laboratório no prazo de até 48 horas, preferencialmente. Material enviado além deste prazo não inviabiliza o procedimento, mas pode gerar artefatos pré analíticos que potencial risco de alterar o procedimento ou exames subsequentes.
Citopatologia de Líquidos e Escarro: O material deve ser enviado em frascos de boca larga para permitir a fácil colocação e retirada do material. O material deve ser encaminhado sem solução fixadora ao laboratório em até 6 horas, devendo ser mantido resfriado em geladeira até o momento do transporte. Não há necessidade de controle de temperatura no transporte, caso o material seja encaminhado neste prazo, após resfriado.
Exceção: caso não seja possível o envio dentro deste prazo, ou caso o envio seja por correio ou transportadora, a partir de município fora de BH, recomenda-se que seja colocado álcool etílico a 96% em quantidade correspondente a cerca de 10% ao volume do material enviado. Neste caso não há necessidade de controle de temperatura no transporte.
Observação: o material coletado e fixado deve ser enviado ao laboratório no prazo de até 24 horas, preferencialmente. Material enviado além deste prazo não inviabiliza o procedimento, mas pode gerar artefatos pré analíticos que potencial risco de alterar o procedimento ou exames subsequentes.
Data e hora da coleta devem ser registradas na requisição de exames, nos casos acima.
Lâminas e blocos para revisão ou imuno-histoquímica devem ser acondicionados em recipientes rígidos para evitar quebras, sem necessidade de solução fixadora. Para transporte, é necessário um recipiente secundário e uma caixa identificada.
Para garantir a integridade do material de empréstimo / Imuno-histoquímica (bloco de parafina e lâmina) durante o transporte, siga as orientações abaixo:
• Lâminas: As lâminas serão armazenadas pelo laboratório em um frasco de plástico rígido ou em um porta-lâminas de material semelhante. Certifique-se de transportar o frasco ou porta-lâminas com cuidado, evitando quedas ou impactos que possam danificar as lâminas.
• Blocos de Parafina: O material fixado em parafina deve ser mantido em um local fresco e em temperatura ambiente durante o transporte. Evite deixar o material exposto ao calor excessivo, como em automóveis sob o sol ou próximo a fontes de calor.
• Obs.: O material acima não gera risco de contaminação.
• Transporte o material diretamente do laboratório para o local de destino, evitando deixá-lo por períodos prolongados em condições inadequadas.
Estas medidas são essenciais para assegurar que o material chegue em perfeitas condições para a realização dos exames necessários.
No ato da retirada de material para realização de exames adicionais e/ou revisão externa, deve ser realizado registro fotográfico no sistema utilizado (imagem da lâmina e/ou bloco de parafina) para garantir a correspondência com a descrição no protocolo assinado pelo paciente.
Para assegurar a rastreabilidade, todas as atividades de coleta, transporte e recebimento devem ser registradas desde a coleta até o descarte. Os registros de transporte devem ser armazenados por, no mínimo, cinco anos, ou conforme legislação específica para cada tipo de MBH. Um checklist deverá ser utilizado para verificar e registrar a adequada rotulagem das caixas de transporte e a conformidade de cada item.
No momento do recebimento, o destinatário deve:
• Registrar as condições do MBH recebido.
• Comunicar a chegada do material ao remetente (caso não seja colaborador da empresa responsável pela coleta).
• Reportar quaisquer inconformidades observadas ao remetente.
• Com o objetivo de aprimorar a segurança das amostras e o controle de rastreabilidade do transporte realizado pelo IMJ, o Instituto Moacyr Junqueira adquiriu tags de identificação fixadas na mala de transporte e no baú da motocicleta de coleta. O uso desses dispositivos possibilita o monitoramento das coletas e a garantia da rastreabilidade das amostras durante todo o trajeto.
• A RDC 978/2025 determina que todo transporte de MBH possua monitoramento das condições ambientais, com controle de temperatura quando aplicável.
• O controle de temperatura aplica-se especialmente aos materiais não fixados (congelações, líquidos, secreções), que devem ser mantidos sob refrigeração até o envio. Nesses casos, o material deve ser transportado em maleta térmica com termômetro acoplado.
Em situações de falha no transporte, perda de amostra ou acidente, o Plano de Contingência do IMJ descrito no Manual da Qualidade deve ser acionado, incluindo comunicação imediata ao setor da qualidade e registro de não conformidade.
Todas as etapas — coleta, acondicionamento, transporte, recebimento e descarte — devem ser registradas no sistema utilizado, assegurando rastreabilidade completa.
Todos os registros de transporte e rastreamento devem ser mantidos por no mínimo cinco anos, conforme determina a legislação vigente.
O remetente é responsável por incluir toda a documentação necessária para o transporte do MBH, assegurando que o transportador tenha acesso às informações exigidas e garantindo o cumprimento de todos os requisitos regulamentares.
O recipiente em contato direto com a amostra deve ser um frasco rígido ou um saco plástico resistente, preferencialmente com sistema de vedação para prevenir vazamentos.
Para amostras líquidas, é fundamental que o frasco seja adequadamente rotulado e, se necessário, envolto em papel absorvente para garantir a contenção de qualquer possível vazamento.
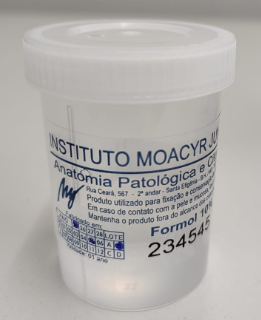



As amostras devem ser colocadas em um recipiente secundário resistente (como uma caixa ou bolsa plástica) que seja hermeticamente fechado.
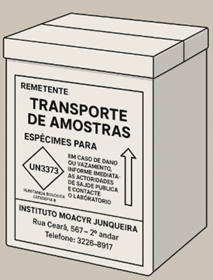
O recipiente terciário deve ser uma maleta rígida e lavável, que deve ser identificada externamente com a designação “substância biológica da categoria B – UN 3373” e os símbolos de “espécimes para diagnóstico”.
A maleta deve conter papel absorvente e uma compressa adicional para o caso de derramamento acidental.

Cada amostra deve ser identificada com etiqueta legível em português, contendo de preferência: nome do paciente, número do frasco, tipo de amostra, e data de coleta.
Uma lista de verificação deve acompanhar as amostras, documentando o estado das amostras e qualquer informação relevante para o transporte.
Realizada pelo colaborador externo no ato da coleta, onde é verificada a conformidade entre a guia de requisição médica e o material coletado.
O representante deve registrar quaisquer discrepâncias imediatamente, e solicitar ao colaborador do remetente responsável a devida correção ou ciência e assinatura.
No laboratório, o responsável pela coleta e o colaborador designado deve comparar o conteúdo da maleta com a lista de verificação, garantindo que todas as amostras estejam presentes e em boas condições.
Um registro de recebimento deve ser feito, incluindo:
Nome do paciente, número da amostra, estado da amostra (adequado, danificado, etc.), e qualquer observação necessária.
Documentação de Recebimento:
O carimbo de conferência deve incluir informações como:
• Acondicionamento adequado
• Ausência de Informação para cadastro
• Devolução/Rejeição (Conforme itens relacionados na planilha de rejeição de amostra) – Em caso de devolução de material o cadastro de devolução no sistema X-Clinic deverá ser realizado.
• “Conferido por” e “data da conferência”.
Todos os colaboradores devem utilizar EPIs adequados (luvas, avental, máscara, protetor facial, conforme o tipo de amostra).
Em caso de acidente, vazamento, derramamento, extravio ou furto, o colaborador deve interromper imediatamente o transporte, isolar o material e comunicar o fato à gerência técnica e ao setor da qualidade.
O Plano de Contingência descrito no Manual da Qualidade define as ações corretivas, responsáveis, prazos e registros de cada incidente, assegurando a rastreabilidade e a comunicação ao responsável técnico e à ANVISA, quando aplicável.
Equipamentos de Proteção e Ações em Caso de Acidente – Uso de EPIs:
▪ Todos os colaboradores envolvidos na coleta e transporte devem utilizar Equipamentos de Proteção Individual (EPIs) adequados, incluindo luvas e se necessário, máscaras.
▪ O motoboy e o representante devem portar pelo menos três pares de luvas e solicitar luvas adicionais conforme a necessidade nos hospitais ou clínicas.
▪ Em caso de acidentes durante o transporte, o colaborador deve usar luvas para manuseio seguro do material biológico e informar imediatamente ao laboratório.
▪ Caso não possa realizar a coleta, a maleta/baú deve conter informações de contato para assistência e um telefone do laboratório.


O representante deve notificar a empresa e registrar um boletim de ocorrência em caso de furto, extravio ou roubo de material, garantindo que os pacientes e médicos sejam informados sobre a situação.
Identificação da Caixa: A caixa de transporte deve ser identificada externamente com nome e endereço do remetente e destinatário, além de símbolos de orientação e riscos. Incluir uma lista de verificação do material biológico transportado e as condições de envio.
Documentação: É necessário que a documentação de transporte seja preenchida com informações sobre as amostras, incluindo nome do paciente, número do frasco e natureza do material biológico. Frases de advertência devem ser incluídas quando aplicável.
Condições de Transporte: Os materiais devem ser transportados em temperatura ambiente, sem necessidade de controle de temperatura durante o transporte, salvo especificações em contrário para determinadas amostras. O controle de temperatura aplica-se especialmente aos materiais não fixados (líquidos, secreções), que devem ser mantidos sob refrigeração até o envio. Nesses casos, o material deve ser transportado sob refrigeração.

Horário e Local da Coleta: A coleta deve ser realizada de segunda a sexta-feira, entre 16:00 e 17:00 horas, conforme contrato de prestação de serviço.
Preparação do Material: Após a conferência do material e cortes, as amostras devem ser acondicionadas em cassetes numerados com a identificação do exame correspondente.
Responsabilidade da Macroscopista: A macroscopista do IMJ deve verificar e contar os cassetes antes do envio para o CEH, documentando no caderno de protocolo as quantidades e condições.

Para realização do exame de imunohistoquímico, o funcionário do IMJ será responsável pela separação dos blocos de parafina conforme solicitação interna. Posteriormente o bloco de parafina é entregue ao patologista juntamente com a lâmina respectiva para separação do bloco adequado para análise, no caso de mais de um bloco. O bloco de parafina juntamente com a solicitação é entregue ao setor digitação para rastreamento no sistema, envio para CEH. O funcionário do CEH é responsável pela retirada, conferência e assinatura da listagem de rastreamento, sendo que uma via fica no IMJ e a outra acompanha a remessa enviada.
O prestador de serviço CEH se responsabilizará pela coleta dos blocos de parafina contendo os materiais para confecção de novas lâminas e realização das reações de imunohistoquímica e pela entrega das mesmas. As lâminas deverão ser entregues montadas com verniz e lamínula, em ordem numérica, etiquetadas e rastreadas no sistema do IMJ com a descrição de técnica liberada. Acesso liberado no sistema apenas com este módulo.
Entrega de Lâminas: As lâminas deverão ser entregues montadas com verniz e lamínula, em ordem numérica, etiquetadas e rastreadas no sistema do IMJ com a descrição de técnica liberada. Acesso liberado no sistema apenas com este módulo. As etiquetas para identificação das lâminas são fornecidas pelo IMJ (na etiqueta consta o código de barra, o nome do paciente, o número do exame), juntamente com o mapa de trabalho. O mapa de trabalho é impresso em duas vias, uma via assinada e devolvida e a outra entregue ao prestador de serviço. A lâmina e o bloco do material processado são entregues no IMJ após 24 horas de seu processamento, exceção apenas para as urgências e prioridades entregues antes de toda a rotina. Os blocos são entregues no setor técnico em ordem crescente, armazenados em bandeja identificada com: BLOCOS PARA CONFERÊNCIA E ARQUIVO. As lâminas são entregues no setor da microscopia acondicionadas em bandeja própria a disposição do patologista.
Se for identificada alguma divergência os setores envolvidos serão comunicados para as devidas análises e tomada de decisão. Uma planilha de registro de não conformidade identificada por alguma falha no processo acordado será registrada. Esse registro será realizado pelos setores técnico e macroscopia no IMJ no ato da conferência dos blocos de parafina entregues.
Todo o processo é registrado no sistema e/ou caderno de protocolo.
Um mapa de trabalho deve acompanhar as lâminas, com uma via sendo devolvida assinada pelo prestador de serviço.
Tratamento de Divergências: Se divergências forem identificadas durante a conferência de lâminas e blocos, os setores envolvidos devem ser notificados imediatamente e um registro de não conformidade deve ser elaborado.
O funcionário do prestador de serviço CEH será responsável pela coleta do material no setor de macroscopia para processamento e confecção das lâminas.
Coleta e Transporte de Blocos: O CEH deve ser responsável pela coleta e transporte dos blocos de parafina e pela confecção de novas lâminas, assegurando que todos os materiais estejam adequadamente identificados e documentados.
Acidente Durante o Transporte: O funcionário designado deve utilizar EPIs para qualquer manuseio de materiais em caso de acidentes durante o transporte, informando aos responsáveis do IMJ para ações corretivas. Todo material coletado é transportado em caixa devidamente identificada do prestador de serviço.
Requisitos de Rotulagem: As etiquetas devem ser claras, legíveis e impressas em português, utilizando tinta indelével e à prova d’água. As informações na etiqueta devem incluir: nome do paciente, número do exame, tipo de material, e informações de contato do laboratório.
Frascos de Acondicionamento: Os frascos devem ser de plástico resistente, com mecanismo de vedação que impeça qualquer vazamento, e devem incluir informações sobre o produto utilizado, como a composição do fixador e medidas de primeiros socorros.
Uma planilha deve ser mantida para registrar o mês, ano e lote de fabricação dos produtos utilizados, com a validade informada claramente.
Remetente: É responsável pelo acondicionamento adequado, documentação para transporte, e comunicação sobre a natureza e características das amostras.
Transportador: Deve garantir que o transporte ocorra em condições adequadas, com infraestrutura necessária para a manutenção da integridade das amostras.
Destinatário: O destinatário é responsável por verificar o recebimento, garantindo que todos os documentos e amostras estejam corretos e completos. O termo de consentimento informado deve ser acessível para consulta.
O recebimento criterioso do material enviado ao laboratório garante o processo adequado das amostras, conforme PRS IMJ 013.
1-Material biológico sem identificação
2-Lâmina quebrada
3-Ausência de amostra biológica e/ou lâmina no frasco
4-Ausência de pedido/ requisição médica
5-Nome do paciente diverge totalmente da solicitação médica e/ou guia.
6-Fracos inadequados e/ou solução fixadora inadequada.
7-Nº de frasco diverge com o descrito na solicitação médica.
8-Convênio não credenciado ao laboratório
9-Paciente em carência para realização do procedimento
10-Discrepância entre pedido do exame e o material enviado
11- Ausência de número do frasco e de nome do paciente no pedido.
Ausência de informação para cadastro/ informação incompleta:
1-Falta de descrição do material/natureza sede na solicitação.
2-Ausência de dados para cadastro (número da carteira)
3-Ausência de assinatura e/ou carimbo do médico solicitante.
4-Nome do paciente diverge em parte da solicitação médica.
5-Outros (especificar);
O Sistema de Gestão da Qualidade (SGQ) do Instituto Moacyr Junqueira é estruturado para assegurar o cumprimento das exigências legais, técnicas e éticas aplicáveis aos serviços de Anatomia Patológica e Citopatologia. Esse sistema visa garantir a rastreabilidade, a padronização dos processos, a melhoria contínua e a segurança diagnóstica, alinhado às diretrizes das RDCs nº 504/21, nº 786/23 e nº 978/25 da ANVISA, bem como às boas práticas laboratoriais da Sociedade Brasileira de Patologia (SBP).
Dentro desse sistema do Instituto Moacyr Junqueira compreende o Controle Interno da Qualidade (CIQ) e o Controle Externo da Qualidade (CEQ), aplicáveis a todas as etapas do processo técnico e administrativo que envolvem o recebimento, processamento, análise e liberação de laudos anatomopatológicos e citopatológicos.
O Controle Interno da Qualidade (CIQ) é realizado de forma contínua e sistemática, garantindo a rastreabilidade dos processos e a conformidade dos resultados com os critérios técnicos estabelecidos e inclui:
• Monitoramento das condições de coleta, transporte e fixação dos espécimes;
• Verificação do desempenho dos equipamentos e reagentes;
• Avaliação da qualidade das lâminas histológicas e citológicas;
• Conferência de registros de amostras, rastreabilidade e integridade dos dados no sistema utilizado;
• Avaliação da conformidade documental de todos os POPs e formulários relacionados.
Os resultados do CIQ são revisados periodicamente pela Gestão da Qualidade e pelo Responsável Técnico e as não conformidades identificadas originam registros necessários e contato com a procedência de origem, conforme os procedimentos internos do SGQ do IMJ.
O Controle Externo da Qualidade (CEQ) é realizado por meio da participação no Programa de Proficiência e Controle de Qualidade (PPCQ) da Sociedade Brasileira de Patologia (SBP), que avalia periodicamente o desempenho técnico do laboratório. Os resultados obtidos são analisados pelo responsável técnico e pela Gestão da Qualidade, servindo de base para:
• Reforço e direcionamento de treinamentos;
• Revisão e atualização de procedimentos;
• Implementação de ações de melhoria contínua.
O IMJ mantém registros atualizados, auditáveis e rastreáveis de todas as atividades relacionadas ao PGQ, incluindo relatórios de avaliação, atas de reuniões de análise crítica, resultados de proficiência e registros de calibração e manutenção de equipamentos.
MBH (Material Biológico Humano): Qualquer material proveniente do corpo humano utilizado para fins diagnósticos, incluindo sangue, fragmentos de tecidos, secreções, líquidos corporais, entre outros.
Acondicionamento Primário: Embalagem em contato direto com o material biológico (ex.: frasco com formol, frasco de citologia líquida, tubo com sangue).
Acondicionamento Secundário: Embalagem intermediária que contém o recipiente primário, capaz de conter vazamentos (ex.: embalagem plástica, saco plástico com material absorvente).
Acondicionamento Terciário: Embalagem externa rígida e lavável, identificada de acordo com as normas, utilizada para transporte seguro do MBH até o laboratório.
Formol 10% tamponado: Solução aquosa composta por 10% de formaldeído, tamponada com fosfato para manter o pH neutro, usada para fixação de amostras histopatológicas.
Requisição de Exames: Documento que acompanha o MBH contendo as informações clínicas, identificação do paciente, tipo de exame solicitado, data e hora da coleta, entre outros.
Artefatos Pré-analíticos: Alterações no material causadas por falhas na coleta, acondicionamento, fixação ou transporte, que podem comprometer a análise laboratorial.
Imuno-histoquímica: Técnica laboratorial que utiliza anticorpos específicos para identificar proteínas em tecidos fixados e incluídos em parafina.
Revisão de Lâminas: Processo de reavaliação de lâminas histológicas ou citológicas previamente analisadas, com ou sem solicitação de exames complementares.
PAAF (Punção Aspirativa por Agulha Fina): Procedimento de coleta de células com agulha fina, geralmente guiado por imagem, para avaliação citopatológica.
Giemsa: Corante usado para coloração de células em amostras citológicas, especialmente útil em amostras secas não fixadas previamente com álcool.
Check-list: Lista de verificação utilizada para assegurar a conformidade dos itens exigidos em determinado processo, como rotulagem e integridade da embalagem.
X-Clinic: Sistema de informação laboratorial utilizado para controle de registros, imagens, rastreabilidade e documentação associada ao MBH.
ANVISA – 2015. Manual de Vigilância Sanitária sobre o Transporte de Material Biológico Humano para fins de Diagnóstico Clínico. Este manual fornece diretrizes para o manejo seguro e adequado de material biológico em situações clínicas.
Manual de Gestão da Qualidade para Laboratório de Citopatologia. Instituto Nacional de Câncer José Alencar Gomes da Silva, Coordenação-Geral de Prevenção e Vigilância, Divisão de Detecção Precoce e Apoio à Organização de Rede – Rio de Janeiro: Inca, 2012. Este manual aborda a gestão da qualidade e práticas recomendadas para laboratórios de citopatologia.
Portaria SMSA-SUS/BH 038/99 de 06 de julho de 1999. Normativa que estabelece diretrizes para o funcionamento dos serviços de saúde pública, incluindo protocolos de manuseio e transporte de materiais biológicos.
RESOLUÇÃO CFM Nº 2.074/2014. Publicada no D.O.U. de 28 de julho de 2014, Seção I, p.91-2. Disciplina as responsabilidades dos médicos e laboratórios de Patologia em relação aos procedimentos diagnósticos de Anatomia Patológica e estabelece normas técnicas para a conservação e transporte de material biológico em relação a esses procedimentos.
RESOLUÇÃO Nº 3665 de 04 de maio de 2011. Agência Nacional de Transportes Terrestres. Regulamento para o Transporte Rodoviário de Produtos Perigosos. Esta resolução define as normas para o transporte de produtos que podem representar riscos à saúde e segurança.
RESOLUÇÃO – RDC Nº 504 de 27 de maio de 2021. Agência Nacional de Vigilância Sanitária. Dispõe sobre as boas práticas para o transporte de material biológico humano, com ênfase em segurança e integridade durante o transporte.
RESOLUÇÃO – RDC Nº 786 de 30 de outubro de 2023. Esta resolução regulamenta o controle e a segurança no transporte de materiais biológicos, reforçando a importância da rastreabilidade e das boas práticas para a integridade do material durante todo o processo de transporte.
RESOLUÇÃO – RDC Nº 978, de 29 de julho de 2025. Estabelece os requisitos sanitários e de qualidade para o funcionamento dos serviços de Anatomia Patológica e Citopatologia, incluindo critérios para infraestrutura, qualificação de pessoal, rastreabilidade, biossegurança e gestão da qualidade.
Requisitos para Acondicionamento e Limpeza de Recipientes Terciários: Lista de verificação e orientações práticas para higienização e rotulagem dos recipientes terciários, conforme exigido pela legislação vigente (documento físico no setor representantes).
Instruções Específicas para Fixação e Envio por Tipo de Exame – www.imj.com.br e/ou www.imj.com.br/coletas e/ou www.imj.com.br/formulario
Procedimento de Empréstimo e Rastreabilidade de Lâminas e Blocos: Fluxo de controle do empréstimo com registro fotográfico no sistema utilizado e assinatura de protocolo pelo paciente (registro realizado no cadastro do paciente em nosso sistema).
Rastreabilidade e Registro de Transporte: planilha utilizada para o transporte (documento Físico no setor Representantes).
Procedimento de Conferência no Recebimento das Amostras: Etapas da conferência inicial e secundária das amostras, incluindo modelo de registro de recebimento e observações necessárias (documento de referência Manual da Qualidade e PRS IMJ 013 – Conferência de Amostras).